Lộ diện tử huyệt của tế bào ung thư
Các nhà khoa học đã xác định được "gót chân Achilles" của tế bào ung thư ác tính, mở ra hy vọng phát triển một loại thuốc mới, nhắm mục tiêu chính xác vào khả năng di căn mà không cần đầu độc các mô khỏe mạnh.
Các nhà khoa học tại Trung tâm Quy luật Hệ gen (CRG) ở Barcelona vừa công bố một khám phá mang tính bước ngoặt, tiết lộ cơ chế phòng thủ chưa từng được biết đến, giúp các tế bào ung thư sống sót và di căn.
Cơ chế phòng thủ của tế bào ung thư
Khám phá cốt lõi nằm ở cách tế bào ung thư phản ứng với sức ép cơ học (physical squeezing). Các nhà nghiên cứu phát hiện ra rằng, khi bị đè nén mạnh - mô phỏng điều kiện chúng phải len lỏi qua các mô khối u dày đặc hoặc chui vào mạch máu - tế bào ung thư sẽ tăng cường cấp phát thêm năng lượng (ATP) một cách nhanh chóng.
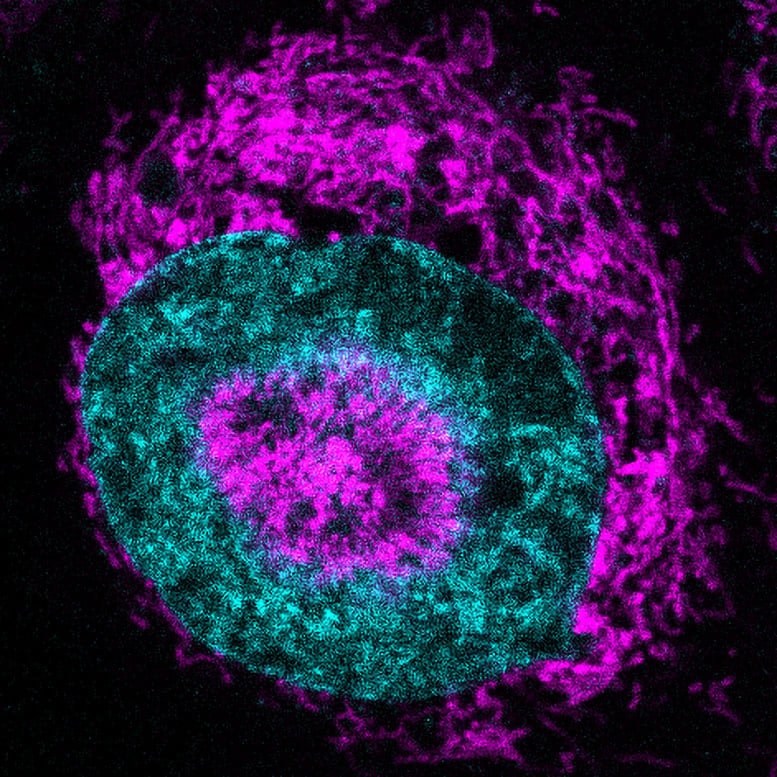
Cụ thể, trong các thí nghiệm, khi nén tế bào HeLa xuống còn khoảng 3µm, ty thể nhanh chóng di chuyển gần nhân tế bào, "cấp phát" thêm nguồn năng lượng tế bào (ATP) ngay lập tức. Cấu trúc này được gọi là "NAMs" (nucleus-associated mitochondria - ty thể liên kết hạt nhân). Hiện tượng này xuất hiện trong khoảng 84% tế bào bị nén, nhưng gần như không thấy ở tế bào "tự do" không chịu áp lực.
Tiến sĩ Sara Sdelci, đồng tác giả nghiên cứu, nhận định điều này buộc giới khoa học phải suy nghĩ lại về vai trò của ty thể. Chúng không chỉ là những thỏi pin tĩnh, mà giống như những lực lượng phản ứng nhanh linh hoạt được triệu tập trong các tình huống khẩn cấp.
Cơ chế giúp ung thư di căn
Tại sao sự tăng cường năng lượng này lại quan trọng? Theo nghiên cứu, sức ép vật lý gây ra tổn thương DNA nghiêm trọng, làm đứt gãy và rối loạn bộ gen. Tế bào cần một lượng ATP khổng lồ để huy động các đội sửa chữa, nới lỏng DNA và tiếp cận các điểm bị hỏng.
Với lượng ATP bổ sung từ NAMs, các tế bào ung thư bị ép có thể sửa chữa DNA trong vòng vài giờ và tiếp tục quá trình phân chia. Ngược lại, những tế bào không nhận được năng lượng tăng cường này sẽ ngừng hoạt động. Khả năng phục hồi này chính là chìa khóa giúp tế bào ung thư vượt qua các thách thức cơ học của môi trường cơ thể, một bước thiết yếu trong quá trình di căn (lan rộng).
Bằng chứng lâm sàng cũng ủng hộ giả thuyết này khi kiểm tra mẫu sinh thiết khối u vú, các nhà nghiên cứu nhận thấy số lượng NAMs ở mặt trước của khối u xâm lấn cao gấp ba lần so với vùng lõi của khối u.
Cắt đứt mạch năng lượng
Các nhà nghiên cứu còn xác định được "giàn giáo" tế bào giúp ty thể di chuyển và cố định quanh hạt nhân. Cấu trúc này bao gồm các sợi Actin (một loại protein quen thuộc giúp cơ bắp co giãn) và Lưới nội chất.
Phát hiện này mở ra một hướng điều trị hoàn toàn mới. Khi các nhà khoa học sử dụng thuốc latrunculin A để phá vỡ các sợi Actin, sự hình thành NAMs đã sụp đổ và dòng năng lượng ATP tăng vọt bị cắt đứt. Điều này cho thấy có thể sử dụng các loại thuốc nhắm mục tiêu vào "giàn giáo" này để ngăn chặn sự tăng cường năng lượng của tế bào ung thư.
Đồng tác giả nghiên cứu, tiến sĩ Verena Ruprecht kết luận rằng phản ứng đối với sức ép cơ học là một điểm yếu chưa được khai thác của tế bào ung thư. Phát hiện này có thể mở ra các con đường trị liệu mới mà không gây hại rộng rãi cho ty thể và các mô khỏe mạnh. Việc nhắm mục tiêu vào cơ chế NAMs có thể là chiến lược hiệu quả để làm cho tế bào ung thư ít xâm lấn hơn và ngăn chặn chúng di căn.
